平成17年度 メチル水銀を中心とした水銀の健康影響と国際的水銀汚染問題に関するレビュー
代表研究者 佐藤 洋(東北大学医学系研究科教授)
研究要旨
「メチル水銀を中心とした水銀の健康影響のレビュー」として、これまでは感受性の高い胎児期曝露の生後の発育発達への影響を中心に据えてきた。しかし、それ以外にも影響があり得るとの論文もいくつか報告されている。そこで本年度は、低濃度メチル水銀曝露と心疾患との関連性に関する報告のレビューについて紹介する。Salonenら(1995)は、低濃度メチル水銀曝露が心疾患と関連するのではないかと、最初に報告していが、その後、2000年と2005年にも同じ研究グループから同一コホート(東部フィンランド)の追跡結果を報告する2論文が出されてきた。さらに、他の地域(ヨーロッパやアメリカ合衆国)からもmulticenter case-control studyやnested case-control studyが報告されてきたので、今回のレビューの対象とした。日本国内では、このような研究は見当たらないが、水俣病患者あるいは水俣病患者が多発した地域の死因を分析した研究についてもレビューした。Salonenらの東部フィンランドにおける研究とGuallarら(2002)のヨーロッパ8カ国とイスラエルにおける症例対照研究の論文だけが、メチル水銀の心臓毒性を示唆する結果であった。Yoshizawaら(2002)は、水銀曝露と心疾患の関連を示唆する結果は無いとした。同様な否定的な結果を出している論文もいくつか見られた。これらの文献を見る限り、今後も急性心筋梗塞などの心疾患の症例対照研究は遂行する必要があるものと考えられた。
キーワード:水銀汚染、メチル水銀、胎児期曝露、心疾患
研究協力者氏名
仲井邦彦(東北大学医学系研究科助教授), 亀尾聡美(東北大学医学系研究科助手), 永沼 章(東北大学薬学研究科教授), 村田勝敬(秋田大学医学部教授), 吉田 稔(聖マリアンナ医科大学助教授), 坂本峰至(国立水俣病研究センター部長), 鈴木恵太(東北大学医学系研究科研究員)
I 研究目的
メチル水銀による健康影響の全貌は科学的に明らかになっておらず、ことに低濃度曝露の影響については、閾値を含めて解明されていない。近年、魚類等に蓄積したメチル水銀の胎児期曝露の児の発育発達への影響に世界的にも関心が集まっており、これらの研究レビューを継続する必要があろう。また、成人における極めて低濃度のメチル水銀曝露と心疾患や動脈硬化との関連も指摘されている。そこで、本研究においては年齢幅の広いスペクトラムでの影響を文献的に概括し、メチル水銀による健康影響の全貌を出来るだけ明らかにすることを目的とする。
Ⅱ 研究方法
メチル水銀を中心とした水銀の健康影響と国際的水銀汚染問題に関する研究レビュー「メチル水銀を中心とした水銀の健康影響のレビュー」および「低濃度メチル水銀曝露と心疾患との関連性に関する報告のレビュー」として、まず、世界各地でどのような報告があるかをMedline等のデータベースから検索・収集した。本年度は、低濃度メチル水銀曝露と心疾患との関連性に関する報告のレビュー」に関して検索された論文の中から中心的な文献について概説を行い、コメントをつけた。
(倫理面への配慮)
倫理面への配慮については、公開された文献の調査、及び調査の視察を中心とする研究であるので特に必要とは思われない。
Ⅲ 研究結果
世界各地でどのような水銀汚染問題があるかについて先ず、文献検索により調査を行った。本年度は、2005年を対象年として、Medlineを対象データベースとして、key words = (mercury or methylmercury)&pollutionで検索した結果、43論文がヒットした。また、key words = (mercury or methylmercury)&(infants or fetus)で検索すると19論文がヒットした。さらに成人において極めて低濃度のメチル水銀曝露と心疾患や動脈硬化との関連が指摘されており、児の発育発達への影響ばかりでなく、生涯にわたる健康影響を視野に入れる必要があると考えられるが、これらの研究レビューの準備のために、key words = (mercury or methylmercury)&cardiovascularで、検索したところ13論文がヒットした。
また学術論文のみではなく、新聞報道等のレビューのための検索準備を始めた。米国のみならずインドネシアなどの発展途上国などの諸外国で発行されている新聞報道などもDialog以外にウェブサイトを用いて検索可能であることを確認した。
本年度は、文献検索の結果と、1996年以前の重要と思われる論文を基に、低濃度メチル水銀曝露と心疾患と関連について概説した。
低濃度メチル水銀曝露と心疾患との関連性に関する報告のレビュー
はじめに
低濃度メチル水銀曝露は、これまで胎児期の曝露とその生後の発達におよぼす影響の可能性というコンテキストの中で議論されてきた。しかし、それ以外にも影響があり得るとの論文もいくつか報告されている。Salonenら(1995)は、低濃度メチル水銀曝露が心疾患と関連するのではないかと、最初に報告した。その後、2000年と2005年にも同じ研究グループから同一コホート(東部フィンランド)の追跡結果を報告する2 論文が出されてきた。さらに、他の地域(ヨーロッパやアメリカ合衆国)からもmulticenter case-control studyやnested case-control studyが報告されてきたので、今回のレビューの対象とする。日本国内では、このような研究は見当たらないが、水俣病患者あるいは水俣病患者が多発した地域の死因を分析した研究があるのであわせてそれらにふれることとする。
1. 東部フィンランドのコホート調査
Salonenらは、東部フィンランドでKuopio Ischemic Heart Disease Risk Factor Study(KIHD)と言われるpopulation-based prospective studyを行っている。東部フィンランドは、魚類摂取量が多いにもかかわらず、冠状動脈疾患(coronary heart disease, CHD)の死亡率が高いことで知られている。彼らは、魚介類中の水銀が急性心筋梗塞(acute miocardial infarction, AMI)をはじめとする冠状動脈疾患による死亡や心血管系疾患(cardio vascular disease, CVD)と関連するとの仮説のもとでいくつかの論文を報告した。
1.1. Salonen et al. (1995)の論文
まず、第一報に当たる論文についてやや詳細に概説記述する。
(論文名)
Salonen et al. (1995). "Intake of mercury from fish, lipid peroxidation, and the risk of myocardial infarction and coronary, cardiovascular, and any death in eastern Finnish men. Circulation 91(3), 645-55.
(対象)
対象集団は、東部フィンランドに住む42 歳から60歳(6歳毎)の男性、1833名調査された集団は、東部フィンランドに住む男性で、(1984年3月から1989年12月に行われた)ベースライン調査時に、42、48、54 あるいは60歳の3,235名からなる。このうち2,682名(82.9%)が参加した。
除外基準は、冠状動脈疾患(677)、脳血管疾患の既往(60)、(間欠性)跛行(108)、がん(46)。”冠状動脈疾患に罹患している者”とは、急性心筋梗塞の既往がある者、狭心症、Rosa interviewで労作性狭心症陽性の者あるいはニトログリセリン錠を週に一度以上服用する者と定義された。除外されずに残った1889名のうち、魚摂取量と毛髪中水銀濃度の両方のデータが得られた1833名が今回の分析の対象だが、そのうち10名の血圧、36名の喫煙歴、47名の血清フェリチン値、61名の血清アポリポプロテインB、72名の血清HDL2コレステロール値、183名の最大酸素摂取量のデータが失われており、今回分析対象者全体の平均値を当てはめた。
(試料等の採取)
飲酒を3日、喫煙と食事を12時間以上避けた後、静脈血採取、毛髪、24時間尿(対象集団の一部)も採取。
(水銀分析法)
硝酸/塩酸を加えて、マイクロウェーブで灰化、過マンガン酸カリで中和後、Sodiumborohaydrateによる還元気化アマルガム法(FIAS-200)で測定。
(その他の検査)
血清リポプロテイン分画(VLDL, LDL及びHDL等)、フェリチン、血清セレン(Zeeman-AASで測定)、血清銅、血漿アスコルビン酸等
(魚介類および水銀摂取量の測定)
採血時に、食事調査が行われた(instructed and interviewed-checked 4-day food recording)。事前に記録の指示があり、提出時に栄養士によってチェックを受けた。水銀や各種栄養素は、NUTRICA(栄養成分のデータで主にフィンランドの値を使っている)によって算出。
(その他のリスクファクター)
喫煙状況、心筋梗塞・狭心症・その他の虚血性心疾患の既往、高血圧罹患、降圧剤服用等はアンケートで問い、後でインタビューによって確認。12ヶ月間のアルコール摂取量(Nordic Alcohol Consumption Inventry)、血圧(5分休息後に、仰臥位3回、立位1回、坐位2回の平均)、最大酸素摂取量と心電図の虚血性変化、狭心症症状、最大心拍数130/分以下
(酸化LDL の測定法)
ウサギの抗血清を使った免疫法
(フォロ−アップ)
Kuopio州は、WHO MONICAプロジェクトによって心筋梗塞等の登録が確立。登録は非死亡性の急性心筋梗塞やその他冠状動脈疾患による死亡を収集。1984年3月から1991年12月までに73例のAMI(死亡および生存)が登録された。1992年末までには78名の死亡(全死因)が登録され、内18名がCHD(ICD 410-414)、24名がCVD(ICD 390-458)であった。AMIの個人の最大追跡期間は7.75年、平均約5年、死亡の最大追跡期間は8.75年、平均約6年であった。
(結果)
曝露の指標
魚介類摂取量 平均46.5g/日(レンジ:0-619.2g)、推定水銀摂取量 平均7.6μg/日(レンジ: 1.1-95.3μg)、毛髪中水銀濃度 平均1.92μg/g(レンジ:0-15.67μg/g)。サブセット207名の24 時間尿中水銀排泄量1.18μg(レンジ:0-4.95μg)。魚介類と水銀の摂取量には、ベースライン検査の年による差は見られなかったが、毛髪中水銀濃度は、2.55、2.47、1.92、1.51、1.40、1.72 と年を経るにしたがって低下した(p<0.001 for linear trend)。以下の解析では検査の年で調整した。
年齢とベースライン検査年で調整後、毛髪中水銀濃度と24時間尿中水銀排泄量(サブセット207名)は相関係数0.563。魚介類摂取量とは、毛髪中水銀濃度で0.265、24時間尿中水銀排泄量で0.470と比較的高かった。毛髪中水銀濃度と低社会経済的地位が相関係数0.210であった(これは?)。29.2%が現在喫煙者で、非喫煙者に比べて毛髪中水銀濃度が有意に高い(2.20と1.81μg/g)。23%が田舎に住み都市居住者に比べて毛髪中水銀濃度が有意に高い(2.46と1.76μg/g)(魚介類摂取量に関しては差があるとの記述はない)。
AMI、CHD、CVD関連イベントの相対リスク
年齢、ベースライン検査年、および虚血性心電図変化と最大酸素摂取量で調整したコックス比例ハザードモデルの結果(表-1、原論文のTable-3)は、AMIでは毛髪中水銀濃度・魚介類摂取量・水銀摂取量が有意に高く、CHDおよびCVDでは毛髪中水銀濃度が有意に高かった(毛髪中水銀濃度および魚介類摂取量に関しては一単位当たりの変化とカットオフ値で群分けした時のRRの記載があるが、水銀摂取量では一単位当たりの変化だけ)。その他のリスクファクターで調整した結果(表-2、原論文のTable-4)も、前述の結果とほぼ同様であった。
サブセットにおけるAMIと24時間尿中水銀排泄量
ベースライン調査時の24時間尿中水銀排泄量とAMI の相対リスクを、水銀測定値のある69名の患者と(2対1で年齢、検査年および居住地をマッチさせた)対照群で検討した(表-3、原論文のTable-5)。患者群では尿中水銀排泄量はやや多い(1.29μg/日、SD=1.14:対照群は1.13+/-1.08)ものの有意差はない。多重ロジスティックモデルでは尿中水銀排泄量が有意であった。
サブセットにおける酸化LDLと水銀や各種プロオキシダント・アンチオキシダント
187名であるが、酸化LDLを含む血清中免疫複合体が測定された。水銀濃度や他の要因との多重回帰分析で毛髪中水銀濃度が免疫複合体のタイターとの関連が最も強かった。
食事調査における摂取魚種と毛髪中水銀濃度
4日間の食事調査で、ある魚種を摂取したと答えた人とそうでない人の平均毛髪中水銀濃度(年齢、検査年、社会経済状態で調整)を示す(表-4、原論文のTable-7)と、4種(Burbot, Vendace, Northern pike, White fish:これも一種の魚でよいか)の魚で摂取したと答えた人はそうでないと答えた人よりも平均毛髪中水銀濃度が有意に高かった。また一部の魚種では居住地が有意となるものがありインターラクションも有意であった魚種も2種あった。なお、魚の摂食量が1日あたり30g以上の人(51.4%)は平均毛髪中水銀濃度が有意に高く、居住地も有意であった。
(当論文に対するコメント)
これらの結果からSalonenらは、魚介類中の水銀が成人男性における心血管イベントに関与しているとし、その機序として水銀による抗酸化作用の減少がフリ−ラジカル産生や脂質過酸化を促進すると考えている。しかし、彼らの考える水銀の脂質過酸化促進のメカニズムは、Fenton-type反応、SH基への高親和性、セレン化水銀の生成であり、これらは無機水銀における現象である。
もうひとつ可能性のある動脈硬化性の影響として、水銀化合物(これが何であるかを確認)が動脈の平滑筋細胞を増殖させ、ADP誘発血小板凝集を増強させるとの実験結果を示している。
著者ら自身でも、この結果は東部フィンランドのように伝統的に肉や魚、飽和脂肪酸に富む獣脂を多く摂取し、セレン、ビタミンCやその他の野菜から摂取される抗酸化物質が少ないという交絡要因の結果だと認めている。しかし、その一方でCHDの病因に新しい情報を付け加えるものともしている。また、別な集団で再検討されるべきだとしている。
元来フィンランドではセレン含有量の低い土壌があり、セレン摂取量の不足がCVD等のリスクファクターであることは、Salonenら自身の論文にも記述されている。この研究では、セレンは測定されているが、その測定結果は記載されていないのも理解に苦しむ。
Salonenらは、水銀によってCVDの死亡率が高まる仮説を記述しているが、メカニズム的にはどれも無機水銀においておきる、過酸化の促進や抗酸化作用の減少である。メチル水銀も生体内で無機化されるが、無機化率はそれほど高くないと考えられている。いったん無機化すると尿中に排泄されるので、尿中水銀は、無機水銀への曝露と無機化した水銀の合計した量と考えられる。その場合、歯科用アマルガムからの発散あるいは遊離した水銀蒸気やイオン型の無機水銀への曝露量が問題になるが、アマルガムの充量は測定されていない。
さらにアルコール摂取量は聞き取りがされているようであるが、特に結果の報告は無く、BMIや肥満に関するデータが無い。これらについては、Cox比例ハザードモデルに交絡要因として入れても意味ある違いにならなかったとしているのみである。
ベースライン調査の年によって毛髪中水銀濃度が異なり、年とともに低下している。そのため、解析では調査の年を調整するひとつの要因にしているが、これについては深いディスカッションは無い。確かに、母集団からランダムにサンプリングしていれば調査の年によって毛髪中水銀濃度が異なるはずはないであろう。しかし、そのような保証は無く、年によって年齢や居住地の違いがあったとも無かったとも、記述されていない。したがって、調査の年を調整するひとつの要因とすることは、水銀測定の結果を歪める可能性があると思われる。
様々な疑問が生じており、これだけの結果からメチル水銀がAMIやCVDのリスクファクターであると結論づけることは困難で、さらに他の集団での研究が必要であろう。
1.2. Rissanen, T. et al. (2000)の論文
Salonenらと同じ集団を対象として主に魚由来の不飽和脂肪酸の影響を論じた論文について概説する。
(論文名)
Rissanen, T., S. Voutilainen, et al. (2000). "Fish oil-derived fatty acids, docosahexaenoic acid and docosapentaenoic acid, and the risk of acute coronary events: the Kuopio ischaemic heart disease risk factor study." Circulation 102(22): 2677-9.
(対象)
対象集団は、Salonen et al. (1995)と同じ集団1871名。追跡期間は、平均10年(1984年3月から1997年12月)。194例の冠状動脈に由来する事故(coronary events)が発生し、100例は明らかな急性心筋梗塞、60例はおそらく急性心筋梗塞と考えられ、34例は典型的な急性の胸痛であった。
(不飽和脂肪酸の測定)
不飽和脂肪酸はキャピラリーガスクロで測定され、DHA(docosapentaenoic acid)とDPA(docosahesaenoic acid)の和の全脂肪酸に対する割合として計算された。
(交絡因子)
交絡因子については、前報の通り。
(結果)
DHA+DPAの割合は、3.01±0.79%SD、範囲は1.39-7.51%)であった。その割合で5群に分けて様々の変数を比較したのが図-1である。冠動脈の事故は、DHA+DPAの割合の最低群で高い。毛髪中水銀濃度は、DHA+DPAの割合の最低群で低く、DHA+DPAの割合の最高群で高い。単にこれだけ見ると、上述のSalonenら(1995)の論文の結論とは合わない。Cox比例ハザードモデルで、年齢、検査年、BMI、最大酸素摂取量、毛髪中水銀濃度、血清フェリチン、血清LDLコレステロール、収縮期血圧、血清インスリン、ADP誘発血小板凝集、社会経済的状態、運動時虚血所見、喫煙、居住地(地方かそれ以外)、エネルギー摂取量で調整すると、DHA+DPAの割合の最低群に比べてDHA+DPAの割合の最高群では44%(95%CI, 11-65%)のリスクの低下が認められた。
この論文の著者らはさらに、毛髪中水銀濃度で3群に分けて、最高濃度群とそれ以下の濃度の2群を層化して比較した。その結果毛髪中水銀最高濃度群でDHA+DPA の割合の最低群に比較して、毛髪中水銀濃度低値群でDHA+DPAの割合の最高群は、67%の冠動脈の事故が減少している(95%CI 19-87%)としている。
(考察)
これらの事実から、この論文の著者らは不飽和脂肪酸の急性冠動脈事故のリスクを減少させる効果を、魚中の水銀が減弱させていると結論づけている。
(コメント)
確かに図-1を見ると毛髪中水銀濃度で層化した二つの群の、DHA+DPAの割合に対する冠動脈の事故のリスクは異なって見える。毛髪中水銀濃度2μg/g以下ではDHA+DPAの割合の上昇にしたがってリスクは下がるように見え、毛髪中水銀濃度2μg/g超では、いったん下がって第3分位群で最低になりそこからまた上昇しているように見える。しかし、このように10の群に分けた場合の(冠動脈事故の)発生数は少ないと予測される。群毎の発生数についての記述は無く、統計的な確かさについて疑問が残る。翻って表を見てみると、DHA+DPAの割合で分けた5群間で、居住地(地方かそれ以外)が大きく異なっている。上述のSalonenら(1995)の論文の結果に対するコメントと同様に、やはり居住地がなんらかの要因であることは考え得る。また、ここでもセレンの測定結果には触れておらず、また歯科用アマルガムの曝露についてもまったく触れていないのが奇異であった。
1.3. Virtanen, J. K. et al. (2005)の論文
同じくSalonenのグループからの論文で、1995年の論文の観察期間を長期化したものが報告されている。
(論文名)
Virtanen, J. K., S. Voutilainen, et al. (2005). "Mercury, fish oils, and risk of acute coronary events and cardiovascular disease, coronary heart disease, and all-cause mortality in men in eastern Finland." Arterioscler Thromb Vasc Biol 25(1): 228-33.
(対象)
対象集団は、Salonen et al. (1995)と同じ集団。追跡期間は、平均13.9年(1984年3月から2002年12月末)。
(毛髪集水銀濃度や不飽和脂肪酸の測定)
前報の通り。
(交絡因子)
交絡因子については、前報の通り。
(フォローアップスタディ)
死亡は、国家死亡登録で個人識別番号によって行われた。すべでの急性冠動脈事故やCVD(cardiovascular disease=ICD9, 390-459 or ICD10, I00-99)CHD(coronary heart disease=ICD9, 410-414 or ICD10, I20-I25)、全死因が含まれている。急性冠動脈事故は、1992年まではMONICA projectの一部として、それ以降は病因登録システムのレコードリンケージで得られた。診断基準は、FINMONICA projectと同一であった。148例の明らかな急性の冠状動脈に由来する事故(acute coronary events)、77例のおそらく急性の冠状動脈に由来する事故(acute coronary events)が発生し、57例の典型的な遷延性胸痛があった。複数回冠状動脈に由来する事故のあった者は最初のものをend pointとした。525例の死亡のうち257例がCVD関連(非関連268例)であった。
(結果)
平均13.9年(レンジは0.3-17.8年)の追跡で、282例の急性の冠状動脈に由来する事故(acute coronary events、観察対象者数=1871)があり、CVD132例(観察対象者数=1842)、CHD91例(観察対象者数=1871)であった。なお、全死因は、観察対象者数2480の内525例であった。表-5(原論文のTable-1)に毛髪中水銀濃度3群に分けた、観察結果とベースライン調査時の変数を示す。急性の冠状動脈に由来する事故をはじめ、各死亡率は毛髪中水銀濃度の最高群で高い(が、観察期間については記述無し)。また、魚の摂取量も高く、喫煙率も高い。その他の変数でいくつか毛髪中水銀濃度の異なる3群の間で(統計学的に有意な)差異のあるものがあるが、値としては大きくは異ならない。また、ここではじめて血清セレンの測定値が提示され毛髪中水銀濃度の異なる3群の間でほぼ同じ値を示した(どの群も117μg/L 台)。
Cox比例ハザードモデルで、年齢、検査年、血清HDLとLDLコレステロール、虚血性心疾患の家族歴、収縮期血圧、BMI、最大酸素摂取量、ニコチン代謝物尿中排泄量、血清セレン、血清DHA+DPA、アルコールをはじめとする飽和脂肪酸摂取量・食物線維・ビタミンC, Eの摂取量で調整すると、毛髪中水銀濃度の最も高い群では低い二つの群に対して、各エンドポイントで1.68から1.38倍のリスクを持つことが示された(表-6、原論文のTable-2)。調整した交絡因子の少ないモデルにおいてもほぼ同様の結果であった。
さらに毛髪中水銀濃度で層化した二つの群の血清DHA+DPAの単位当たりのエンドポイントの相対リスク値の上昇と毛髪中水銀濃度と血清DHA+DPAの交絡作用を示している(表-7、原論文のTable-3)。
(考察)
これらの結果から、毛髪中水銀濃度は(CVDやCHDを含む)急性冠状動脈事故と関連し、メチル水銀(摂取)が不飽和脂肪酸の急性冠状動脈事故の減少効果を打ち消すとしている。
(コメント)
この論文の表-5にはいくつか疑問がある。No. of events (n [% of subjects])であるが、観察対象者数がそれぞれ異なるとは言え、%で表された数字が必ずしも正しくないように思われる。Acute coronary event (282)とCHD death(91)は観察対象者数=1871 で、No. of subjectsの624+625+622の和と相応する。しかし、毛髪中水銀濃度の最高群の128 (29.6%)は、誤りで、もし128が正しいならば20.58%(128÷622×100)のはずで29.6%とは大きく異なる。CVD death (132)は観察対象者数=1842 であり毛髪水銀レベルの異なる3 つの群のNo. of subjects は、必ずしも明らかでない。しかし、7.0%、4.8%、9.8%は、No. of subjects を624、625、622 として計算した時の割合と最大0.32%程度しか異ならない。理解しにくいのは、Any death (525)の 115 (16.7%) 124 (17.2%) 286 (26.8%)の割合である。%の値から毛髪中水銀濃度の異なる3群の人数を計算すると、689、721、1067 となり、総計は2477でほぼ著者らの言う2480例と合致する。しかし、なぜ、毛髪中水銀濃度の最高群だけが、400名以上も増加しているのか、不思議な感じがすることを否めない。ちなみに表-7では、毛髪中水銀濃度最高群1068名、それ以下の2群の合計は1412名とほぼ上記の計算(689+721=1410)と一致する。
また、観察対象者数1871名とあるが、Salonenら(1995)の魚摂取量と毛髪中水銀濃度の両方のデータが得られた1833名より増えているのも何故か?ベースライン時の調査の結果が、どの対象数に基づいているのかこの表では不明瞭である。
このように細かく表を見てみると理解しにくいことが何点かある。また、この論文では前2報で問題にしていた居住地(都会か田舎か)について何も触れていないのも不思議である。
2. 東部フィンランド以外のヨーロッパあるいはアメリカ合衆国の調査
Salonenらのグループの3論文は、いずれも同じ地域住民男性のコホートであるが、その他にいくつか異なった地域での調査もある。
2.1. Guallar, E. et al. (2002)の論文
(論文名)
Guallar, E., M. I. Sanz-Gallardo, et al. (2002). "Mercury, fish oils, and the risk of myocardial infarction.[see comment]." New England Journal of Medicine 347(22): 1747-54.
(概説)
Guallarら(2002)の論文は、ヨーロッパ8カ国とイスラエルでの症例対照研究である。70歳以下のはじめて心筋梗塞を診断された男性684名と724名の(同一地域からの)対照の足爪の水銀濃度と皮下脂肪のdocosahexaenoic acid(DHA)を測定した。足爪の水銀濃度の平均は、0.25μg/gでありDHAレベルと他の冠状動脈疾患のリスクファクターを調整した後の患者群の水銀濃度は対照群よりも15%(95%信頼区間5-25%)高かった。また、足爪の水銀濃度で5群に分けリスク(odds ratio)を検討すると、水銀濃度最高群は最低群に比べて2.16(95%CI: 1.05-4.29、体位、喫煙、飲酒、HDLコレステロール。糖尿病、高血圧罹患歴、心筋梗塞家族歴、抗酸化物質濃度等で調整後)であった。逆にDHA レベルで群に分け水銀濃度で調整しリスク(odds ratio)を検討するとDHA レベル最高群は、最低群に対して0.59(95%CI: 0.30-1.19)であった。
これらの結果からGuallarらは足爪の水銀濃度は直接的に心筋梗塞のリスクと関連し、DHAはAMIのリスクを下げるとしている。
(コメント)
Guallarら(2002)の論文では足爪の水銀濃度を曝露指標にしているが、毛髪水銀や血中水銀ほどその意味は解明されていない。また魚摂取量も無いので解釈は難しい。歯科用アマルガムからの水銀が影響しないのかも、疑念が残るところでる。しかし、水銀とDHA濃度にそこそこの相関がある(r=0.34)ことも事実である。また、症例と対照の水銀濃度の違い(最大の比で1.33、最小で0.85)より、地域の水銀濃度の違いの方が遥かに大きい(地域の平均で最小は0.15μg/g、最大は0.68μg/g)のも気になるところである。
全体的には、しかし、フィンランド東部のコホート研究をサポートする結果になるとも言えよう。
2.2. Yoshizawa, K. et al. (2002)の論文
異なった結果を報じている論文もある。
(論文名)
Yoshizawa, K., E. B. Rimm, et al. (2002). "Mercury and the risk of coronary heart disease in men.[see comment]." New England Journal of Medicine 347(22): 1755-60.
(対象)
Yoshizawaら(2002)は、歯科医が半分以上を占める医療関係者(男性のみ)のコホート調査から、心疾患のnested case-control studyを行った。
対象者は登録時の1986年に45-75歳の男性、歯科医の他、獣医の多い集団。足爪の水銀濃度を測定。2年毎の郵送の質問紙あるいは応答の無かったものはNational Death Indexで1992年1月末日(5年のフォロ−アップ)までに94%以上の健康状態を把握。症例は、致死的冠状動脈疾患(突然死45名を含む109名)、非致死的急性心筋梗塞(234名)、冠状動脈バイパス手術あるいは経皮的経管的冠状動脈形成術を受けた者(あわせて127名)の470名であった。年齢、喫煙習慣、足爪の提出時期で対照を選定した。
(結果)
足爪の水銀濃度は、症例群0.74±1.21μg/g、対照群0.72±1.40μg/gと差はなかった。表-8(原論文のTable-2)に足爪の水銀濃度のよって5群に分けた時の年齢、喫煙等で調整した相対リスクを示すが、水銀濃度との関連は見いだされなかった。さらに(どのようにしてデータを得たかについて記述されてはいないが)n-3不飽和脂肪酸(EPA+DHA)で調整しても結果は変わらなかった。また、足爪のセレン濃度の高、中、低の3カテゴリーに層化した検討では、セレンの高いカテゴリーでの水銀濃度最高群の相対リスクは同じセレン濃度のカテゴリーの水銀濃度最低群に対して、上昇(2.47、95%CI=1.01-6.04)していたが、trendは有意でなかった。歯科医師は水銀蒸気に曝露されているので有意に水銀濃度が高く、それを除いて解析を行ったが、水銀濃度最高群の最低群に対する相対リスクは、1.27(95%CI=0.62-2.59)であった。
これらのことから、この論文の著者らは水銀曝露と冠疾患の関連を示唆する結果では無いとしている。
(コメント)
突然死が多くの場合、心臓の事故であるとして、致死的冠状動脈疾患(109名で内突然死45名)に分類しているが、若干乱暴のように思われる。また、対象者は保健医療の専門家であり、その意味では健康習慣等も良いと想像するに難くない。これは、Salonenらのグループの研究では、社会階層が低い方がCVDのリスクが高いと思われるようなデータを出していることと、大きく異なっている点である。もし、社会階層が高く健康習慣も良好であるような対象者たちでは、メチル水銀の影響が見えないとすると、Salonenらのグループの研究で見えていたメチル水銀の影響は、メチル水銀そのものでなく何か別の要因の影響であり、メチル水銀はsurrogateであるのかもしれない。足爪の水銀濃度は、症例群0.74±1.21μg/g、対照群0.72±1.40μg/gと差がなかっただけでなく、Guallarら(2002)の論文の足爪水銀濃度(地域の平均で最小は0.15μg/g、最大は0.68μg/g)に比べてかなり高い。CVDの発症率の比較は出来ないが一般には曝露の高い方がより影響が見えやすいと考えられるので、Yoshizawaら(2002)の結果はそれなりの意味を持つものと考えられる。
2.3. Hallgren, C. G. et al. (2001)の論文
これまでは、男性のみでの検討であったが、次のスウェーデンの報告は、女性も含まれている。
(論文名)
Hallgren, C. G., G. Hallmans, et al. (2001). "Markers of high fish intake are associated with decreased risk of a first myocardial infarction." British Journal of Nutrition 86(3): 397-404.
(概説)
Hallgrenら(2001)は、北部スウェーデンの地域住民コホートからはじめての心筋梗塞の症例をMONICA incidence registryから探して症例対照研究を行った。10年の観察期間で78(男62、女16)例の初発心筋梗塞があり、性、年齢、地域をそろえた対照156を選択した。水銀曝露は赤血球中水銀濃度を測定(いつ測定したか確認)し、平均とSDは症例4.4±3.8ng/g、対照5.4±5.9ng/gであった。これらの平均値は、全血の2-3μg/L程度(毛髪中では1ppm以下と思われる)に相当する。n-3不飽和脂肪酸(EPA+DHA)も測定されて血漿中多価不飽和脂肪酸に対する割合として計算された。表に各変数のロジスティック回帰の結果を示す(表-9、原論文のTable-3)が、赤血球中水銀濃度の上昇は心筋梗塞のオッズレシオ(OR)を低下させている。多変量ロジスティック回帰分析(表-10、原論文のTable-4)でも、赤血球中水銀濃度、n-3不飽和脂肪酸割合、その二つの変数の組み合わせのどれも心筋梗塞のOR の低下と関連した。
これらの結果からこの論文の著者らは心筋梗塞のリスクと魚摂取のバイオマーカーである赤血球中水銀濃度と不飽和脂肪酸は逆方向の関連があるとしている。
(コメント)
表-9(原論文のTable-3)で学歴が短い者のORが高いのが著しく目立っている(もっとも教育歴が長い症例が極端に少ないのと症例対照ともにデータの無い例が1割前後あるのが気になるが)。Salonenらのグループの研究でも、田舎に住んでいる者のリスクが高いことがあらわれていたが、生活の仕方が関連するのではないかと思われる。もっとも表-10(原論文のTable-4)の脚注では教育歴は(血清コレステロールや拡張期血圧とともに)有意な寄与は無いとされている。これまで記述して来た論文の対象者はすべて男性であったので、女性の入った研究は意義が深いものと思われる。しかし、数が少ない点もありこの結果からは女性が男性に比べてメチル水銀の心血管系の影響に感受性が高いのかそうでないのかはわからない。
3. 水俣病患者あるいはその多発地域の住民の死因調査
上記の論文での対象者は、一般環境で生活しておりメチル水銀の曝露が必ずしも高くない集団である。Tamashiroらは、水俣病患者あるいは水俣病発生地域住民の死亡を調べる研究報告を行った。これは、より高濃度の曝露集団における結果を示すものと考えられる。
3.1. Tamashiro, H., H. Akagi, et al.(1984)の論文
(論文名)
Tamashiro, H., H. Akagi, et al. (1984). "Causes of death in Minamata disease: analysis of death certificates." International Archives of Occupational & Environmental Health 54(2): 135-46.
(概説)
Tamashiroら(1984)は、水俣病患者と対照の死亡小票から死因の解析を行った。1980年12月までに熊本県には1422名(男799名、女643名)の水俣病患者が認定され、378名が既に死亡していた。このうち1954-1969年に死亡した者44名(典型的な急性水俣病と考えられる)と1970年以降に死亡した慢性水俣病と考えられる者334名(男212、女122)を分けて解析。1970年以降の死亡者には性、死亡年齢(3歳以内)、死亡年(暦)をあわせた同地域の対照をほぼ10500から668名選択した。死因(ICD9に基づく)は、原死因(underlying cause of death)、死亡小票にある死因すべて(multiple causes of death)、二次的死因(secondary causes of death、死亡小票にある死因のうち原死因を除くすべて)に分けて解析。また、水俣病患者群で死因に水俣病の記載が有るか無いかと他の死因の記載の有無が関連しているかどうかも解析した。
(結果)
ここでは、1970年以降の解析についてのみ示す。男女あわせた原死因の分析では、脳血管疾患(18%)、悪性腫瘍(14.7%)、心疾患(虚血性[ICD9 410-414]および非虚血性[ICD9 415-429]あわせて14.1%)、水俣病(14.1%)が多い死因であった。対照では、悪性腫瘍(20.1%)、脳血管疾患(19.6%)、心疾患(虚血性および非虚血性あわせて15.0%)が多い死因であった。オッズレシオは、気管支炎、肺気腫および喘息(ICD9 490-493)の0.41から、腎炎およびネフローゼ(ICD9 580-589)の3.00であったが、どれも95%信頼限界は1をはさんでいた。心血管系疾患(虚血性)のオッズレシオは男では1.32(95%CI=0.57-3.07)、女では0.65(95%CI=0.18-2.28)、心疾患(非虚血性)男では1.31(95%CI=0.71-2.40)、女では2.00(95%CI=0.93-4.28)であった。二次的死因および死因すべて(患者群で609および943の死因が記載)の解析結果を以下に示す。二次的死因の解析では、男女合わせて心疾患(虚血性1.5%および非虚血性19.5%、あわせて21%)が一番多く、対照(815の死因が記載)の心疾患(虚血性1.5%および非虚血性23.3%、あわせて24.8%)とほぼ同一であった。死因すべての解析でも、男女合わせて心疾患(虚血性3.0%および非虚血性15.6%、あわせて18.6%)が一番多く、対照(1483の死因が記載)の心疾患(虚血性3.6%および非虚血性16.7%、あわせて20.3%)とほぼ同一であった。水俣病の記載の有無と他の死因の記載の有無の関連では、心疾患(非虚血性)の男女あわせた結果だけが統計学的に有意な関連を示した。
この論文の著者らは、(ここでは紹介しなかった)1970年以前の死亡者の死因の分布と比べて、1970年以降の死亡者の死因の分布は対照との差が著しくはなかったとしている。
3.2. Tamashiro, H., M. Arakaki, et al. (1986) の論文
(論文名)
Tamashiro, H., M. Arakaki, et al. (1986). "Methylmercury exposure and mortality in southern Japan: a close look at causes of death." Journal of Epidemiology & Community Health 40(2): 181-5.
(対象)
Tamashiroら(1986)は、水俣病患者が集中して発生した水俣市の2地区(熊本県の患者の約70%が居住、また住民の毛髪中水銀濃度も高い)の死因を調査した。1975年の国勢調査で3887人おり1970-1981年の間に416(男女別の数字の計では412で、その後の解析では全死因で412となっているので、416は誤りであろう)の死亡が確認された(男女別では1869と2018、死亡数では216と196)。水俣全市の5歳階級別の死亡率(1972-1978)からStandardised motality ratios (SMR)を計算した。
(結果)
心疾患(ICD9 393-398, 410-429)のSMRは、68.4(95%CI=50.4-92.9)、虚血性心疾患(ICD9 410-414)は、42.9(95%CI=26.9-82.5)と有意に低かった。男女別では、男は有意に低く、女は低い傾向にあった。有意に高いSMR を示したのは、肝臓のがん(ICD9 155)のSMR 207.3(95%CI=116.0-341.9)で男女別では、男のSMR 250.5(95%CI=133.4-428.4)のみ有意であった。脳血管疾患では脳出血(ICD9 431-432)のSMR 166.5(95%CI=124.0-223.5)が有意に高く、男女別では女のSMR 181.9(95%CI=114.0-275.3)のみ有意であった。梗塞はむしろ有意に低くSMR 19.6(95%CI=4.0-57.3)で男女別にわけても有意に低かった。慢性肝疾患と肝硬変(ICD9 571)のSMR は216.0(95%CI=144.1-316.5)と有意に高く、男女別では男のSMR 244.1(95%CI=136.6-402.6)のみ有意であった。その他老衰のSMR 233.6(95%CI=167.2-326.4)が有意に高く、男女別にしても有意であった。また当然のことながら中毒(メチル水銀中毒)のSMR 148.3(95%CI=111.9-196.6)も男女計でのみ有意であった。
これらの結果から論文の著者らは、慢性肝疾患と肝硬変とメチル水銀曝露の関係については他の要因も考える必要があろうとしている。というのは、この地域はアルコールの摂取量の多い地域であり、動物実験もメチル水銀の毒性を強めるとの結果もあるからだとしている。また、脳出血が多いのも脳血管の病理学的変化の報告と一致するとはしているものの、心血管疾患が増えるかもしれないとの予測については、慎重であるべきとしている。現にこの研究では虚血性心疾患のSMRはむしろ低くなっている。
(コメント)
Tamashiroらの研究は、水俣病患者やその多発地域の死因の解析であり、CVDのリスクを対象としたものではない。しかし、より曝露の高い集団での死因の解析で心疾患は対照に比べて多くはなく、一貫して高いSMRを示したのは慢性肝疾患や肝硬変であった。このことは、一般住民に比べて曝露が高い集団の結果であるので、重要視すべきものと考えられる。但し、対照群が同一の市内(ないしは近隣の町村)から選択されていることは問題になり得る。それは、曝露の面から言えば、類似の曝露(つまり対照集団も他の地域の住民に比べればより高い曝露)を受けていることになり、差を出しにくくしている可能性があるからである。しかし、実際には心疾患並びに虚血性心疾患のSMRが低いことから、inverted U(逆U字)のようなかたちの量反応関係を想定しない限り、問題にはならないであろう。
4. アマゾン川流域住民についての調査
Dorea, J. G., R. de Souza Jurandir, et al (2005)の論文
(論文名)
Dorea, J. G., R. de Souza Jurandir, et al (2005).”Hair mercury (signature of fish consumption) and cardiovascular risk in Munduruku and Kayabi Indians of Amazonia.” Environmental Research 97:209-219
(概説)
Doreaら(2005)は、アマゾン川流域のMundurukuとKayabiの原住民における魚消費の指標となる毛髪水銀値と心血管影響について調査研究を報告している。
アマゾン川流域では、金採掘に伴う大気、河川等の水銀汚染が進行し、国際的な問題となっている。砂金抽出の際に使用される金属水銀の環境中への放出により、無機水銀から有機化したメチル水銀が魚介類へ蓄積することで、金採掘労働者の無機水銀による健康被害のみならず、河川に沿って生活し、主要なタンパク源、食糧源を魚に依存している住民において、魚介類を介したメチル水銀の健康被害も懸念されている。そこでDoreaら(2005)は、東部アマゾン川流域のMundurukuの3つの村(Terra Preta, Kaburua, Cururu)とKayabiの1つの村の原住民(インディアン)における魚消費の指標となる毛髪水銀値と心血管影響について調査研究を行った。
(対象)
アマゾン川上流のTapajos川流域で調査を行い、Terra Preta(site1:Tropas川)、Kaburua(site2:Cabitutu川)、Missao Cururu(site3:Cururu川)、Kayabi(site4:TelesPires・Cururuzinho川)の原住民(インディアン)の成人男女、及び子供の計621人を対象として行われた。
(検査項目)
身長、体重、血圧(5分休息後に坐位にて測定)、心拍数、水銀中毒症状の有無
(試料等の採取)
静脈血採取、毛髪(後頭部の頭皮に近い部分)、調査地域で獲れる魚(肉食性、草食性)
(水銀分析法)
硝酸/塩酸を加えて、マイクロウェーブで灰化、冷原子吸光光度法(CV-AAS)で測定
(魚消費率の算出)
魚消費率(g/day)=毛髪総水銀濃度/(魚中水銀濃度×a×b) Richardoson and Currieら(1993)の用いた値を使用:a=0.0010, b=292
(交絡因子)
熱帯特有のマラリア等の感染症の有病率が高い(55.4%)
(結果)
曝露の指標
魚中水銀濃度は、肉食性魚;平均578.6ng/g、草食性魚;平均52.8ng/g であり、全体の魚中水銀濃度は、500ng/g以上が26%、1000ng/g以上が11%であった。毛髪中平均水銀濃度は、Munduruku; 3.4±1.9μg/g、Kayabi; 12.8±7.0μg/g であった。魚平均消費量は、Munduruku;30±16.6g/day、Kayabi; 110±60.6g/dayであった。Kayabiの方が Mundurukuよりも魚摂取頻度・量が多い為、毛髪水銀値が高くなっていると考えられた。肉食性で大型の魚類を好んで食べる地域は、毛髪水銀濃度は高くなるため、地域ごとの生活習慣が大きく影響する。また、魚摂取の指標となる毛髪総水銀濃度と赤血球水銀濃度の関係は、Kayabiの成人で、有意な正の相関が見られた(r=0.5181;P=0,0001)。
肥満度(BMI:body mass index)
Mundurukuの3つの村とKayabi村においてBMI(25以上で肥満)を比較したが、体型には大きな差はなく、有意差もみられず、BMI 25以上の人もほとんどいなかった。
血圧と年齢
Munduruku(収縮期:決定係数0.008、p=0.3368;拡張期:決定係数0.025、p=0.2841)とKayabi(収縮期:決定係数0.025、p=0.2841;拡張期:決定係数0.001、p=0.799)において考えられるすべての年齢で血圧との有意差はなかったが、Kayabiにおいて血圧と年齢による上昇関係はMundurukuより少なかった。
血圧と毛髪水銀濃度
Munduruku(収縮期:決定係数0.044、p=0.0017;拡張期:決定係数0.158、p<0.001)とKayabi(収縮期:決定係数0.014、p=0.4268;拡張期:決定係数0.086、p=0.045)においてMundurukuの方が、収縮期、拡張期とも有意に上昇する傾向があった。
(コメント)
これらの結果を考察すると、Kayabiの成人で、魚摂取の指標となる毛髪総水銀濃度と赤血球水銀濃度の関係が有意な正の相関が見られたことから、Kayabiでは魚介類摂取によるメチル水銀が体内に蓄積していることが示唆された。BMIの結果からは、肥満という心血管疾患のリスクファクターは考えられない。血圧と毛髪水銀濃度の結果をみてみると、魚消費の多いKayabiの方が、リスクが下がるという結果が見られた。これらの結果から、著者らは、魚消費が心血管予防に良いと記述していた、しかしながら、血圧のみをエンドポイントとしている点、またΩ-3不飽和脂肪酸量、LDL、HDL値や喫煙、飲酒等のデータ不足や医療設備の不十分さ、部族間の生活習慣の違い、マラリア等の感染症などさまざまな交絡要因があり、正確な水銀と心血管影響のリスク評価には至っていないと考えられた。
Ⅳ 考察
個々の論文に関するコメントは、それぞれの論文の後に記述した。ここでは、メチル水銀の心臓毒性についてのStern (2005)の総説(1.3.で言及したVirtanen, J. K. et al. (2005)の論文以外について上記の論文のレビューを行っている)についても触れ、全体的なコメントを記述する。
いくつかの疑問はあるものの、Salonenらのグループの東部フィンランドのコホート研究とGuallarら(2002)の論文は、メチル水銀曝露と心臓毒性が関連するとの結果を示したものと考えられる。しかし、その他の論文は、否定的な結果を示していると考えられる。Sternの総説の結論は、Tamashiro et al. (1984, 1986)の論文も含めて全体としては疫学研究が、メチル水銀曝露と急性心筋梗塞のような心疾患との関連を示唆するものであるとしている。しかし、その結論はあまり根拠があるようには思われない。
Sternは、Yoshizawaらの研究とHallgren, et al. (2001)の研究が、否定的な結果であると考えている。その理由として、Yoshizawaらの研究が異なった結果を出しているのは、対象集団に歯科医が多く水銀蒸気曝露があるからではないかとしている。また、Hallgren, et al. (2001)については、数が少なく、ことに水銀濃度が高く不飽和脂肪酸割合の低い者が少ないので限界があるとしている。また、心疾患(cardiac event)のおきる何年も前のメチル水銀曝露の指標を使っているので、誤分類の危険性に注意しなければいけないとしている。
これらのコメントには、いくつか議論すべき点があろう。まず、Yoshizawaらの研究結果については、水銀蒸気曝露が心疾患の発生に影響しているとすれば、歯科医師のグループを入れた解析で水銀曝露(水銀蒸気も含めて)の影響が見え、除いた解析で見えなく(あるいは見えにくく)なるのではないかと考えられる。逆に、メチル水銀曝露に拮抗するとすれば、Sternの言うとおりであろうが、その根拠となるような事象が報告されていない。Stern自身の記述も単に可能性について述べているだけである。
Tamashiro et al. (1984, 1986)の論文も、死因の解析であるがこれらの結果がメチル水銀曝露によって心疾患が増加することを示唆するとは考えにくい。しかし、Sternは否定的な結論を出しているのは上記のYoshizawa らの研究とHallgren, et al. (2001)の研究だけであると考えている。
逆に本稿の著者は、Salonenらの東部フィンランドにおける研究とGuallarら(2002)の論文だけが、メチル水銀の心臓毒性を示唆する結果と考えており、その他の結果は否定的であると考える。
Salonenらの東部フィンランドにおける研究では、前述のように毛髪中水銀濃度と低社会経済的地位が相関することや田舎に住む者が都市居住者に比べて毛髪中水銀濃度が有意に高いことは、気になるところである。居住地(あるいはそれで示される何か別の要因)が影響を与えている可能性も否定出来ない。
次に我が国の現状と、Salonen らの対象集団の特性を比較してみる。
まず曝露要因を考えてみる。魚介類摂取量の平均46.5g/日は、我が国の平均のほぼ半分、推定水銀摂取量の平均7.6μg/日は、ほぼ厚労省のトータルダイエットスタディの平均8μg/日にほぼ匹敵する。毛髪中水銀濃度の平均1.92μg/gは、日本人集団に比べるとやや低いと考えられる。24 時間尿中水銀排泄量1.18μgは、直接比較は出来ないが、22-39歳の男性130人の平均値2.33(SD:1.50)μg/L、比重調整後2.19(SD:1.15)μg/L、クレアチニン補正1.51(SD:0.68)μg/g creatinine に比べてやや低いと考えられる。曝露量の分布は示されていないが、曝露の少ない人 がいる一方で、かなりの高曝露群がおり平均値を上昇させている可能性がある。また、魚介類中の水銀濃度は、やや高めなのではないかと推測される。Salonenら自身が述べているのは、曝露の高い人は地元の湖でとれるlean fishを摂食していることである。それに対して我が国では海に棲む大型魚類(マグロやメカジキあるいはサメ等)が主な曝露源と考えられ、lean fishとは言えない。
次に影響要因では、心疾患の死亡率を比較する。2001年の統計(国民衛生の動向第50巻、2003)で我が国での5歳年齢階級別死亡率(10万対)は、40-44歳で14.3、45-49歳で24.4、50-54歳で38.7、55-59歳で60.3、60-64歳で91.9、65-69歳で151.6である。この6つの年齢階級の死亡率をそれぞれの平均としてして計算すると63.5となる。Salonenらの対象集団では、CVDでの死亡が1833名中24名であり、平均6年追跡期間であるので、単純に計算すると年間の死亡率(10万対)は218.2である。したがって我が国に比べて3倍以上心疾患の死亡リスクが高いことになる。勿論、心疾患の定義と彼らのCVDがどのように重なるのか、あるいは違いはあるのか、我が国のデータでは年齢階級の死亡率の平均を算出したが、それが適当か、またSalonenらの対象集団では登録時の年齢が42から6歳おきに60歳までとなっているが年齢構成は不明である等、直接我が国の死亡率に比較可能かどうかは疑問が残る。しかし、CVDの死亡率が我が国よりかなり高いことは事実であろう。
この二つの要因の違いを考えると、東部フィンランドの結果をそのまま日本にあてはめて同様なことが起きているとは言えないであろう。Salonenら自身は、居住地(田舎)と(低い)社会経済的状態がより多量の魚を摂取させる要因と考えているようだが、それら自体がCVDのリスク要因でもあり、医療へのアクセスの困難さを通してより多い死亡に寄与する可能性がある。
Salonenらの考える水銀の脂質過酸化促進のメカニズムは、Fenton-type反応であり、その他SH 基への高親和性、セレン化水銀の生成が抗酸化作用を抑制するので心疾患が増加すると考えているようである。ただし、これらの現象は無機水銀でおきることである。Sternも基本的には脂質過酸化促進が心疾患を促進するものと考えているようである。ただし、Sternは、神経細胞にメチル水銀を作用させたin vitroの実験に言及して酸化ストレスや反応性酸素種の発生について述べるとともに、その他の毒性発現メカニズムとして、マイクロチューブリンへの影響、カルシウム恒常性の障害、グルタミン系ニューロトランスミッターの増強についても可能性を指摘している。これらの現象が心臓毒性とどうかかわるかについての考察はない。
Doreaらは、アマゾン川流域住民についての調査において、魚消費が心血管予防に良いと記述していたが、諸要因のデータ不足や医療設備の不十分さ、部族間の生活習慣の違い、マラリア等の感染症などさまざまな交絡要因があり、正確な水銀と心血管影響のリスク評価には至っていないと考えられる。
Ⅴ 結論
Salonenらの東部フィンランドにおける研究とGuallarら(2002)の論文が、メチル水銀の心臓毒性を示唆する結果を出した。今回のレビューの結論としては、東部フィンランドにおいてはSalonenのグループが主張するように、メチル水銀曝露の高い人に心筋梗塞等がより高頻度に発生することは言えるかもしれないが、それが普遍的なことであるとは言い難い。Guallarら(2002)の論文は、爪の水銀濃度を指標としており、地域の水銀濃度の方に症例と対照との差よりも大きな違いがあるので評価は難しい。いずれにしてもSalonenらの言う毛髪中水銀レベルが2ppm超で心疾患のリスクがあがるとすると、日本人男性では平均値が2ppmを超えているので何らかの事象がおきているはずである。しかし、そのような調査研究はなされておらず、とりあえず急性心筋梗塞の症例対照研究は遂行する必要があるのかもしれない。
Ⅵ 次年度以降の計画
16-17年度に引き続き、国際的水銀汚染問題・メチル水銀の健康影響に関して報告している文献を、検索・収集する。金採掘等においては、水銀蒸気曝露も懸念されていることから、メチル水銀だけでなく水銀蒸気の健康影響についても視野にいれる。16-17年度と18年度で検索したこれらの文献についてのレビューを行う。また従来の研究で、世界のいくつかの国や地域での実態を明らかにしてきたが、その中で、地域経済との関連は切り離せない問題であることが判明したので、単に環境問題や作業者の健康問題として扱うだけでなく、水銀による健康問題や環境汚染が地域でどのように理解され、住民がどのように考えているかをも明らかにする必要があると考えられた。そこで、18年度では、学術論文で公表後、マスコミでどのように取り上げられたか等の新聞・マスコミ報道の経緯等も含めた上での水銀汚染問題に関するレビューを行う。「メチル水銀を中心とした水銀の健康影響のレビュー」としては、これまで感受性の高い胎児期曝露の生後の発育発達への影響を中心に据えてきたが、本年度は、成人において低濃度のメチル水銀曝露と心疾患や動脈硬化との関連性についてレビューした。今後も、児の発育発達への影響ばかりでなく、生涯にわたる健康影響を視野に入れる必要があると考えられ、これらの研究レビューも引き続き行う予定である。
表-1
Salonen et al. (1995).Circulation 91(3), 645-55.
Table 3. Age-and Coronary Disease‒Adjusted Relative Risks1 of Acute Myocardial Infarction and Death From Coronary Heart Disease, Cardiovascular Disease, or Any Cause Associated With Hair Mercury Content as Well as Dietary Fish and Mercury Intakes
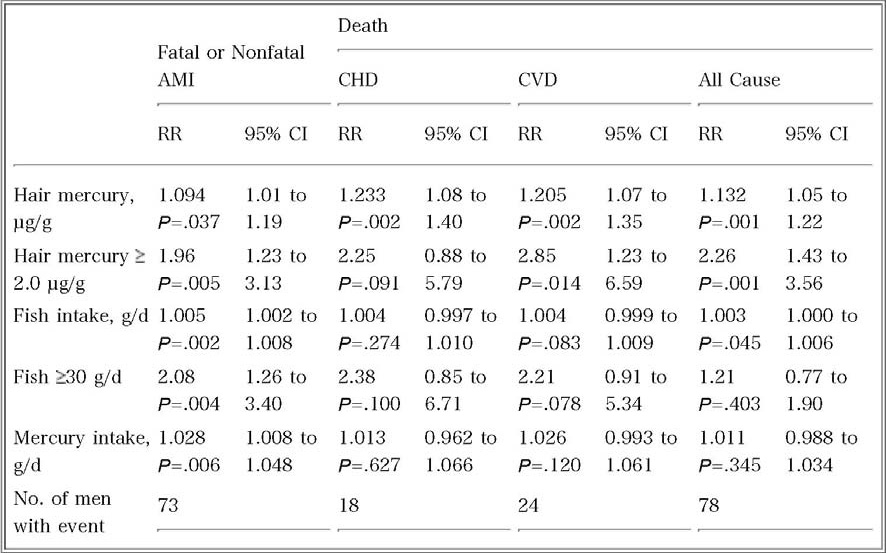
AMI indicates acute myocardial infarction; CHD, coronary heart disease; CVD, cardiovascular disease; RR, relative risk; and CI, confidence interval.
1From multivariate Cox proportional hazards models including age, examination year (five dummy variables), ischemic exercise ECG, and maximal oxygen uptake. n=1833.
表-2
Salonen et al. (1995).Circulation 91(3), 645-55.
Table 4. Risk Factor‒Adjusted Relative Risks1 of Acute Myocardial Infarction and Death From Coronary Heart Disease, Cardiovascular Disease, or Any Cause Associated With Hair Mercury Content as Well as Dietary Fish and Mercury Intakes
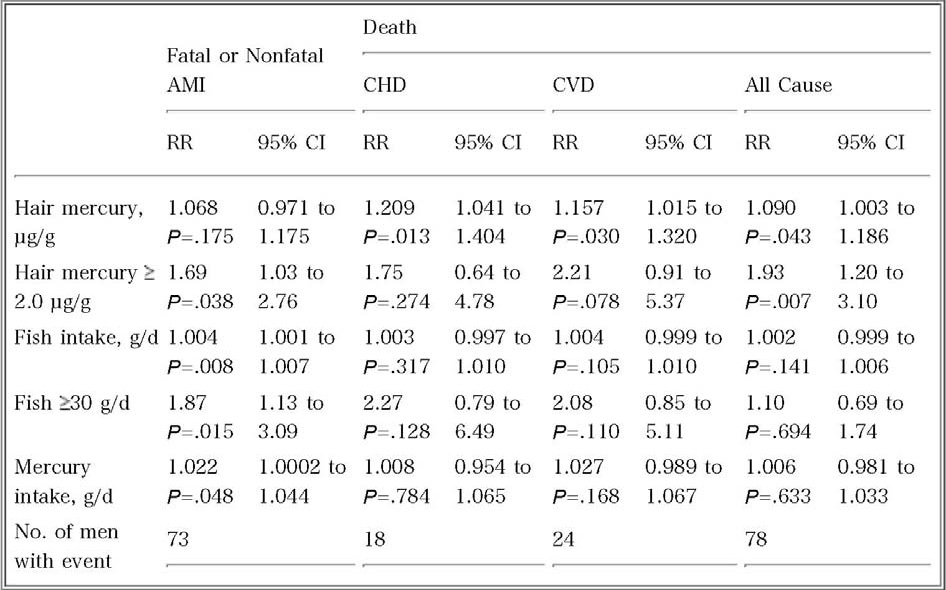
1 From multivariate Cox proportional hazards models including age, examination year (five dummies), ischemic exercise ECG, maximal oxygen uptake, family history of CHD, cigarette-years, mean systolic blood pressure, diabetes, socioeconomic status, place of residence (urban vs. rural), dietary iron intake, and serum apolipoprotein B, HDL2 cholesterol, and ferritin (> vs. <200 μg/L) concentrations. n=1833.
表-3
Salonen et al. (1995).Circulation 91(3), 645-55.
Table 5. Association of 24-Hour Urinary Mercury Excretion and Other Coronary Risk Factors With the Risk of Acute Myocardial Infarction in a Multivariate Logistic Model in 69 Patients and 138 Control Subjects Matched for Age, Place of Residence, and Date of Examination
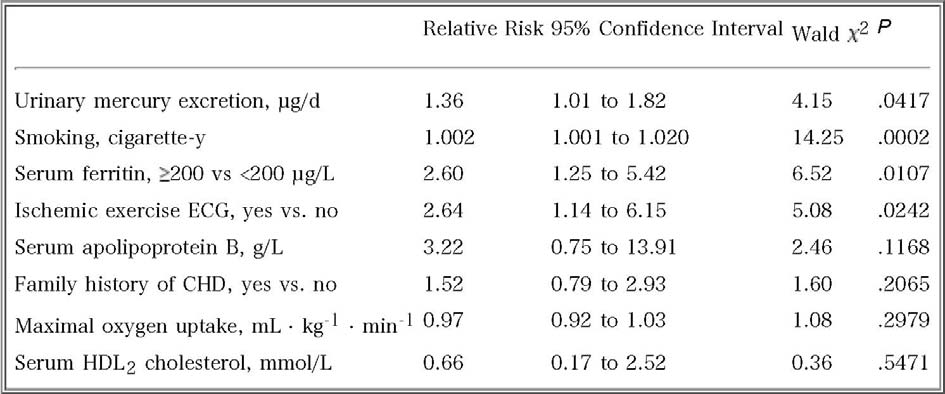
CHD indicates coronary heart disease.
表-4
Salonen et al. (1995).Circulation 91(3), 645-55.
Table 7. Age-and Socioeconomic Status-Adjusted Mean1 Hair Mercury Content in Men Who Reported Use of Various Fish Species During 4-Day Food Recording and in Those Who Did Not, According to Place of Residence
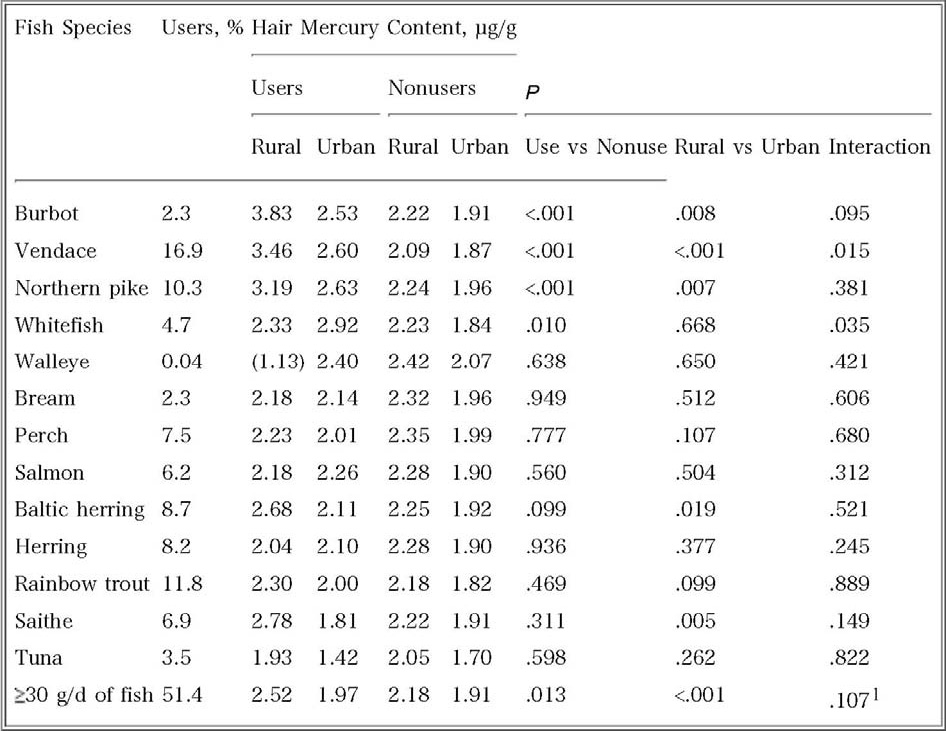
1 Adjusted for age (y), examination year (five dummy variables), and socioeconomic status in two-way ANCOVA.
Smoking-fish interaction from a three-way ANCOVA; P=.064 for a greater difference between users and nonusers in smokers than in nonsmokers.
図-1
Rissanen, T., S. Voutilainen, et al. (2000). Circulation 102(22): 2677-9.
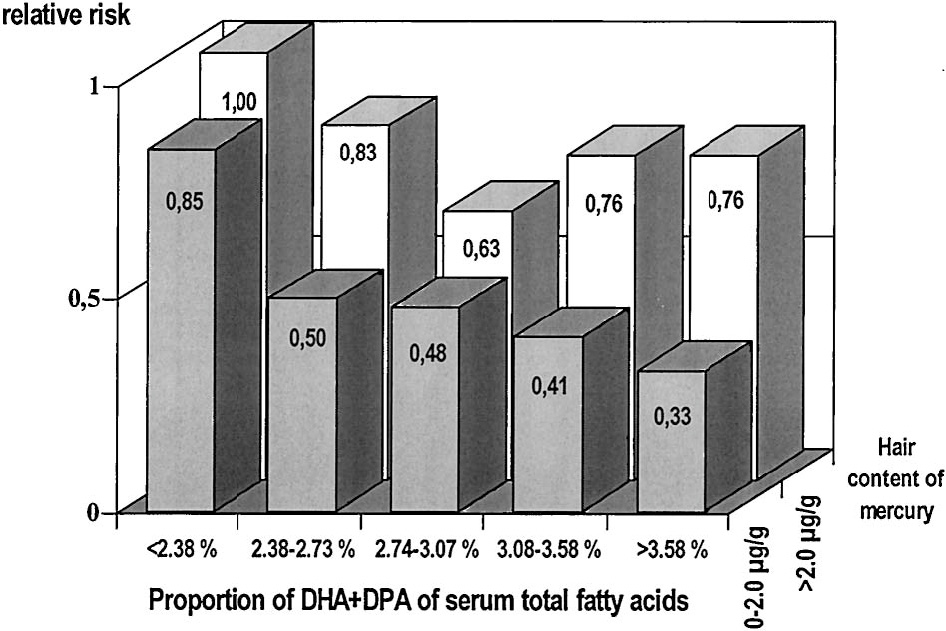
表-5
Virtanen, J. K., S. Voutilainen, et al. (2005). Arterioscler Thromb Vasc Biol 25(1): 228-33
| Characteristic | Hair Mercury Content (μg/g) | P for Heterogeneity | ||
|---|---|---|---|---|
| <0.84 | 0.84-2.03 | 2.03 | ||
| All values are means (±SD) | ||||
| * Counted from 1871 men free of CHD at baseline; †counted from 1842 men from free of CHD or stroke at baseline;
‡counted from 2480 men; § 4-day mean; ¶ measured from 1856 men; # measured from 1693 men; ** measured from 1851 men. |
||||
| NO. of subjects | 624 | 625 | 622 | |
| NO. of events(n [ % of subjects]) | ||||
| Acute coronary event (282)* | 72(11.5%) | 82(13.1%) | 128(29.6%) | <0.001 |
| CVD death (132)† | 43(7.0%) | 30(4.8%) | 59(9.8%) | 0.002 |
| CHD death (91)* | 30(4.8%) | 20(3.2%) | 41(6.6%) | 0.021 |
| Any death (525)‡ | 115(16.7%) | 124(17.2%) | 286(26.8%) | <0.001 |
| Nutritional factors | ||||
| Fish intake (g per day)§ | 30(38) | 43(47) | 65(67) | <0.001 |
| Fiber intake (g per day)¶ | 25.5(9.1) | 25.2(8.8) | 25.5(8.5) | NS |
| Saturated fatty acid intake (% of total energy)¶ | 17.5(4.0) | 17.7(4.0) | 18.4(4.3) | <0.001 |
| Vitamin C intake (mg per day)¶ | 74.6(49.5) | 75.2(53.1) | 73.8(55.1) | NS |
| Vitamin E intake (mg per day)¶ | 9.2(2.9) | 9.1(3.1) | 8.9(3.0) | NS |
| Alcohol intake (g per week) | 66(118) | 76(120) | 78(111) | NS |
| Biochemical and other risk factors | ||||
| Age (years) | 51.2(5.8) | 52.3(5.3) | 53.7(4.5) | <0.001 |
| BMI (Kg/m2) | 26.4(3.3) | 26.8(3.4) | 27.1(3.7) | 0.001 |
| Systolic blood pressure (mm Hg) | 134(16) | 134(16) | 136(17) | 0.028 |
| Diastolic blood pressure (mm Hg) | 89(10) | 89(11) | 90(11) | NS |
| Fasting serum insulin (mU/L) | 10.9(6.7) | 11.1(6.4) | 11.5(6.9) | NS |
| Fasting blood glucose (mmol/L) | 4.7(1.0) | 4.7(0.8) | 4.8(1.0) | NS |
| Serum total cholesterol (mmol/L) | 5.70(1.02) | 5.81(1.06) | 6.08(1.04) | <0.001 |
| Serum LDL cholesterol (mmol/L) | 3.85(0.94) | 3.94(0.97) | 4.22(1.00) | <0.001 |
| Serum HDL cholesterol (mmol/L) | 1.26(0.27) | 1.30(0.29) | 1.34(0.31) | <0.001 |
| Serum triglycerides (mmol/L) | 1.31(0.75) | 1.27(0.77) | 1.22(0.74) | NS |
| Maximal oxygen uptake (L per minute)# | 2.6(0.6) | 2.6(0.6) | 2.5(0.6) | 0.020 |
| Urea nicotine metabolites (mg per day) | 5.8(10.1) | 5.0(9.1) | 6.2(9.2) | NS |
| Serum selenium (μg/L)** | 117.2(16.5) | 117.4(19.3) | 117.0(17.6) | NS |
| Serum DHA+DPA (% of total fatty acids) | 2.74(0.68) | 3.04(0.72) | 3.26(0.86) | <0.001 |
| Percentage of total | ||||
| Smokers (%) | 29.1 | 26.1 | 34.6 | 0.004 |
| Hypertension (%) | 30.8 | 30.0 | 34.9 | NS |
| Diabetes (%) | 3.0 | 4.2 | 5.1 | NS |
| Family history of ischemic heart disease (%) | 44.1 | 47.4 | 46.3 | NS |
表-6
Virtanen, J. K., S. Voutilainen, et al. (2005). Arterioscler Thromb Vasc Biol 25(1): 228-33
| Lowest Third RR |
Middle Third RR (95% CI) |
Highest Third RR (95% CI) |
P for Trend |
Highest vs Lowest Two Thirds Combined RR (95% CI) |
|
|---|---|---|---|---|---|
| * Adjusted for age examination years; † adjusted for model 1 and HDL and LDL cholesterol,BMI, family history of ischemic heart disease, sysytolic blood pressure, maximal oxygen uptake, urinary excretion of nicotione metabolites serum selenium, and alcohol intake; ‡ adjust for model 2 and serum DHA+DPA as proportion of all fatty acids in serum; § adjusted for model 3 and intake of saturated fatty acids,fiber and vitamins C and E. | |||||
| Incidence of acute coronary event | |||||
| Model 1* | 1 | 1.02(0.74−1.41) | 1.61(1.20−2.17) | 0.001 | 1.59(1.25−2.03) |
| Model 2† | 1 | 1.04(0.75−1.44) | 1.55(1.14−2.11) | 0.003 | 1.52(1.19−1.94) |
| Model 3‡ | 1 | 1.08(0.77−1.50) | 1.67(1.22−2.30) | 0.001 | 1.60(1.24−2.06) |
| Model 4§ | 1 | 1.07(0.77−1.49) | 1.66(1.20−2.29) | 0.001 | 1.60(1.24−2.06) |
| Incidence of CVD death | |||||
| Model 1* | 1 | 0.65(0.40−1.04) | 1.24(0.83−1.87) | 0.213 | 1.53(1.08−2.18) |
| Model 2† | 1 | 0.61(0.38−0.99) | 1.17(0.77−1.79) | 0.364 | 1.49(1.04−2.15) |
| Model 3‡ | 1 | 0.67(0.41−1.08) | 1.36(0.88−2.11) | 0.126 | 1.67(1.15−2.43) |
| Model 4§ | 1 | 0.66(0.41−1.07) | 1.35(0.87−2.11) | 0.141 | 1.68(1.15−2.44) |
| Incidence of CHD death | |||||
| Model 1* | 1 | 0.59(0.33−1.05) | 1.17(0.72−1.89) | 0.416 | 1.50(0.99−2.29) |
| Model 2† | 1 | 0.57(0.32−1.03) | 1.07(0.65−1.77) | 0.650 | 1.41(0.91−2.18) |
| Model 3‡ | 1 | 0.63(0.35−1.13) | 1.27(0.75−2.16) | 0.296 | 1.61(1.03−2.53) |
| Model 4§ | 1 | 0.61(0.34−1.10) | 1.21(0.71−2.06) | 0.398 | 1.56(0.99−2.46) |
| Incidence of any death | |||||
| Model 1* | 1 | 0.93(0.72−1.20) | 1.36(1.09−1.70) | 0.001 | 1.41(1.19−1.69) |
| Model 2† | 1 | 0.88(0.68−1.14) | 1.23(0.98−1.54) | 0.025 | 1.31(1.10−1.57) |
| Model 3‡ | 1 | 0.92(0.71−1.19) | 1.30(1.03−1.65) | 0.007 | 1.37(1.14−1.64) |
| Model 4§ | 1 | 0.92(0.71−1.19) | 1.31(1.03−1.66) | 0.007 | 1.38(1.15−1.66) |
表-7
Virtanen, J. K., S. Voutilainen, et al. (2005). Arterioscler Thromb Vasc Biol 25(1): 228-33
| RR (95% CI)* | No. of Cases (% in group) |
P for Interaction Betseen Hair Hg and DHA+DPA |
|
|---|---|---|---|
| * Adjusted for age, examination year, serum HDL and LDL cholesterol, family history of ischaemic heart systolic blood pressure, BMI, maximal oxygen uptake,urinary excretion of nicotione metabolites, serum se hair mercury, alcohol, saturated fatty acids, fiber and vitamin C and E intake. | |||
| Acute coronary event | 0.023 | ||
| Hair Hg <2.03 μg/g (n=1249) | 0.69(0.52−0.91) | 154 (12.3) | |
| Hair Hg 2.03 μg/g (n=622) | 1.06( 0.85−1.32) | 128 (20.6) | |
| CVD death | 0.067 | ||
| Hair Hg <2.03 μg/g (n=1237) | 0.59( 0.39−0.89) | 73 (5.9) | |
| Hair Hg 2.03 μg/g (n=605) | 0.87( 0.61−1.23) | 59 (9.8) | |
| CHD death | 0.005 | ||
| Hair Hg <2.03 μg/g (n=1249) | 0.43( 0.25−0.74) | 50 (4.0) | |
| Hair Hg 2.03 μg/g (n=622) | 1.05( 0.72−1.53) | 41 (6.6) | |
| Any death | 0.836 | ||
| Hair Hg <2.03 μg/g (n=1412) | 0.90( 0.74−1.10) | 239 (16.9) | |
| Hair Hg 2 .03 μg/g (n=1068) | 0.87( 0.74−1.02) | 286 (26.8) | |
表-8
Yoshizawa,K., E.B.Rimm, et al. (2002) New England Journal of Medicine347(22):1755-60
| MEASURE* | QUINTILE OF MERCURY LEVEL | P FOR TREND† |
||||
|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | ||
| * RR denotes relative risk, and CI confidence interval. † The P value was calculated from a test for trend across quintiles. ‡ The lowest quintile of toenail mercury level served as the reference category. § Values have been adjusted for age (six categories:Š50,51 to 55, 56 to 60, 61 to 65, 66 to 70, and >70 years) and smoking (four categories: never smoked, former smoker, 1 to 24 cigarettes daily, and >24 cigarettes daily). ¶ Values have been adjusted for age (six categories:Š 50,51 to 55, 56 to 60, 61 to 65, 66 to 70, and >70 years) and smoking (four categories: never smoked, former smoker, 1 to 24 cigarettes daily, and >24 cigarettes daily), alcohol intake ( four cat 1.0 to 5.0, 5.1 to 30.0, and >30.0 g per dday),family history of coronary heart disease (binary), high blood pressure (binary hypercholesterolemia(binary), diabetes(binary), body-mass index (five categorids) at the 1986 base line, and quintile of to sample weight. # Values have been adjusted for the covariates listed above and also for quintiles of intake of n-3 fatty acids (eicosapentae and docosahexaenooic acid). |
||||||
| Mercury level in toenails — μg /g | ||||||
| Median | 0.15 | 0.28 | 0.45 | 0.67 | 1.34 | |
| Range | 0.03-0.21 | 0.22-0.35 | 0.36-0.54 | 0.55-0.86 | 0.87-14.56 | |
| No. of patients (n=470) | 101 | 93 | 90 | 90 | 96 | |
| No. of controls (n=464) | 85 | 94 | 97 | 97 | 91 | |
| Age- and somking -adjusted RR (95% CI)ठ| 1.00 | 0.83 (0.55-1.25) |
0.77 (0.51-1.16) |
0.77 (0.51-1.16) |
0.87 (0.57-1.31) |
0.83 |
| Multivariate RR (95% CI)ঠ| 1.00 | 0.92 (0.60-1.41) |
0.80 (0.52-1.24) |
0.92 (0.60-1.41) |
0.97 (0.63-1.50) |
0.78 |
| Multivariate RR (95% CI)‡# | 1.00 | 0.93 (0.60-1.43) |
0.83 (0.53-1.30) |
0.96 (0.62-1.51) |
1.03 (0.65-1.65) |
0.55 |
表-9
Hallgren, C.G., G. Hallmans, et al. (2001). British Journal of Nutrition 86(3): 397-404
| Factor | Category | n | OR | 95% CI | Test for linear trend: P = | |
|---|---|---|---|---|---|---|
| Cases | Control subjects* | |||||
| OR, odds ratio; Ery-Hg, Hg level in erythrocytes; P-PUFA, sum concentration of n -3 polyunsatyrated fatty acids 20:5 and 22:6 in blood plasma phospholipids; Ery-GSH-Px,glutathione peroxidase activity in blood. * In total seventy-eight casses and 156 control subjects were included; however, information was not complete. † When Ery-Hg was collapsed into a dichotomous factor (≤6v. >6 ) 0R was 0.45(95% Cl 0.22, 0.92). ‡ When P-PUFA was dichotomised (≤5.5 v. >5.5 ) 0R was 0.43(95% Cl 0.24, 0.79). § When serum cholesterol was dichotomised (≤7 v. >7 ) 0R was 1.61(95% Cl 0.91, 2.86). # When BMI was dichotomised (≤25 v. >25 ) 0R was 2.50(95% Cl 1.32, 4.72). ¶ When diastolic blood pressure was dichotomised (≤90 v. >90 ) 0R was1.82(95% Cl 0.98, 3.39). |
||||||
| Fatty fish consumption (meals/week) | <1 | 56 | 109 | 1.0 | - | |
| ≥1 | 20 | 44 | 0.85 | 0.45, 1.62 | ||
| Lean fish consumption (meals/week) | <1 | 52 | 95 | 1.0 | - | |
| ≥1 | 24 | 58 | 0.76 | 0.42, 1.36 | ||
| Ery-Hg (ng Hg/g erythrocyte)† | ≤3 | 27 | 43 | 1.0 | - | |
| 3-6 | 39 | 68 | 0.91 | 0.49, 1.69 | ||
| >6 | 12 | 44 | 0.43 | 0.19, 0.95 | 0.07 | |
| P-PUFA (%)‡ | ≤5.5 | 38 | 49 | 1.0 | - | |
| 5.5-6.5 | 13 | 41 | 0.44 | 0.21, 0.94 | ||
| >6.5 | 19 | 51 | 0.43 | 0.21, 0.88 | 0.02 | |
| Ery-GSH-Px (μkatal/g heamoglobin) | ≤1 | 18 | 35 | 1.0 | - | |
| 1.0-1.5 | 50 | 97 | 1.00 | 0.52, 1.94 | ||
| >1.5 | 10 | 23 | 0.80 | 0.31, 2.06 | ||
| Serum cholesterol (nmol/l)§ | ≤6 | 25 | 59 | 1.0 | - | 0.05 |
| 6-7 | 20 | 40 | 0.99 | 0.49, 2.00 | ||
| >7 | 33 | 49 | 1.61 | 0.84, 3.09 | ||
| Smoking status | Non-smoker | 39 | 107 | 1.0 | - | |
| Smoker | 30 | 41 | 2.01 | 1.00, 3.59 | ||
| BMI (kg/m2)# | <25 | 23 | 78 | 1.0 | - | |
| 25-28 | 22 | 43 | 1.95 | 0.92, 4.16 | ||
| >28 | 29 | 35 | 3.03 | 1.49, 6.16 | 0.007 | |
| Diastolic blood pressure (mmHg)¶ | <80 | 14 | 45 | 1.0 | - | |
| 80-90 | 26 | 57 | 1.11 | 0.67, 3.22 | ||
| >90 | 35 | 54 | 2.34 | 1.05, 5.23 | 0.09 | |
| Education (years) | >>12 | 2 | 18 | 1.0 | - | |
| ≤12 | 67 | 126 | 4.70 | 1.06, 20.7 | ||
表-10
Hallgren, C.G., G. Hallmans, et al. (2001). British Journal of Nutrition 86(3): 397-404
| Category | Model 1* | Model 2† | Model 3‡ | ||||
|---|---|---|---|---|---|---|---|
| OR | 95% CI | OR | 95% CI | OR | 95% CI | ||
| OR, odds ratio; Ery-Hg, Hg level in erythrocytes; P-PUFA, sum concentration of n -3 polyunsatyrated fatty acids 20:5 and 22:6 in blood plasma phospholipids. * Ery-Hg and P-PUFA considerded as two independent factors in the same model. The interaction between these two factors was tested by likellihood ratio test(P =0.10).Thus, there was a tendency for a multiplicative interaction effect between these two factors (in contrast to model 2). † Ery-Hg x P-PUFA considerded as one factor ( each individual was classified according to his or her Ery-Hg and P-PUFA).The numbers of individuals(casses:control subjects)in each category were: ≤6 and ≤5.5,:34:42; ≤6 and >5.5, 26:60; >6 and ≤5.5, 4:6; >6 and >5.5,6:32. ‡ Ery-Hg x P-PUFA, smoking status and BMI considered as three independent factors in the same model. The factors serum cholesterol, diastolic blood pressure and education did not contribute significantly to the model (test for linear trend; P =0.5, P =0.16 and P =0.9 respectively). |
|||||||
| Ery-Hg (ng Hg/g erythrocyte) | ≤6 | 1 | - | ||||
| >6 | 0.51 | 0.21, 1.24 | |||||
| P-PUFA (%) | ≤5.5 | 1 | - | ||||
| >5.5 | 0.49 | 0.26, 0.91 | |||||
| Ery-Hg x P-PUFA | ≤6 and ≤5.5 | 1.0 | - | 1.0 | - | ||
| ≤6 and >5.5 | 0.58 | 0.30, 1.11 | 0.87 | 0.37, 2.02 | |||
| >6 and ≤5.5 | 1.46 | 0.31, 6.94 | 1.09 | 0.19, 6.23 | |||
| >6 and >5.5 | 0.18 | 0.06, 0.56 | 0.16 | 0.04, 0.65 | |||
| Smoking status | Non-smoker | 1.0 | - | ||||
| Smoker | 2.20 | 0.95, 5.10 | |||||
| BMI (kg/m2) | ≤25 | 1.0 | - | ||||
| >25 | 3.62 | 1.44, 9.15 | |||||
参考文献
- Salonen et al. (1995). "Intake of mercury from fish, lipid peroxidation, and the risk of myocardial infarction and coronary, cardiovascular, and any death in eastern Finnish men. Circulation 91(3), 645-55. http://www.ncbi.nlm.nih.gov/pubmed/7828289
- Rissanen, T., S. Voutilainen, et al. (2000). "Fish oil-derived fatty acids, docosahexaenoic acid and docosapentaenoic acid, and the risk of acute coronary events: the Kuopio ischaemic heart disease risk factor study." Circulation 102(22): 2677-9. http://www.ncbi.nlm.nih.gov/pubmed/11094031
- Virtanen, J. K., S. Voutilainen, et al. (2005). "Mercury, fish oils, and risk of acute coronary events and cardiovascular disease, coronary heart disease, and all-cause mortality in men in eastern Finland." Arterioscler Thromb Vasc Biol 25(1): 228-33 http://www.ncbi.nlm.nih.gov/pubmed/15539625
- Guallar, E., M. I. Sanz-Gallardo, et al. (2002). "Mercury, fish oils, and the risk of myocardial infarction.[see comment]." New England Journal of Medicine 347(22): 1747-54. http://www.ncbi.nlm.nih.gov/pubmed/12456850
- Yoshizawa, K., E. B. Rimm, et al. (2002). "Mercury and the risk of coronary heart disease in men.[see comment]." New England Journal of Medicine 347(22): 1755-60 http://www.ncbi.nlm.nih.gov/pubmed/12456851
- Hallgren, C. G., G. Hallmans, et al. (2001). "Markers of high fish intake are associated with decreased risk of a first myocardial infarction." British Journal of Nutrition 86(3): 397-404. http://www.ncbi.nlm.nih.gov/pubmed/11570992
- Tamashiro, H., H. Akagi, et al. (1984). "Causes of death in Minamata disease: analysis of death certificates." International Archives of Occupational & Environmental Health 54(2): 135-46. http://www.ncbi.nlm.nih.gov/pubmed/6480121
- Tamashiro, H., M. Arakaki, et al. (1986). "Methylmercury exposure and mortality in southern Japan: a close look at causes of death." Journal of Epidemiology & Community Health 40(2): 181-5. http://www.ncbi.nlm.nih.gov/pubmed/3746182
- Dorea, J. G., R. de Souza Jurandir, et al (2005).”Hair mercury (signature of fish consumption) and cardiovascular risk in Munduruku and Kayabi Indians of Amazonia.” Environmental Research 97:209-219 http://www.ncbi.nlm.nih.gov/pubmed/15533337
- Stern, A.H. A review of the studies of the cardiovascular health effects of methylmercury with consideration of their suitability for risk assessment, Environmental Research 2005; 98(1): 133-42 http://www.ncbi.nlm.nih.gov/pubmed/15721894